بررسی MINI
پایگاه ضد سرطان: نشانگرهای جهانی فقط سرطان
Chengchen Qian1، Xiaolong Zou2، Wei Li1،3، Yinshan Li4، Wenqiang Yu5
1Shanghai Epiprobe Biotechnology Co., Ltd, Shanghai 200233, China;2 گروه جراحی عمومی، اولین بیمارستان وابسته دانشگاه پزشکی هاربین، هاربین 150001، چین.3Shandong Epiprobe Medical Laboratory Co., Ltd, Heze 274108, China;4 بیمارستان مردم منطقه خودمختار نینگشیا هوی، دانشگاه پزشکی نینگشیا، یینچوان 750002، چین.5 مرکز بالینی سلامت عمومی شانگهای و بخش جراحی عمومی، بیمارستان Huashan و موسسه متاستاز سرطان و آزمایشگاه اپی ژنتیک RNA، موسسات علوم زیست پزشکی، کالج پزشکی شانگهای، دانشگاه فودان، شانگهای 200032، چین
خلاصه
سرطان عامل اصلی مرگ و میر در سراسر جهان است.تشخیص زودهنگام سرطان می تواند مرگ و میر همه انواع سرطان را کاهش دهد.با این حال، بیومارکرهای موثر تشخیص زودهنگام برای اکثر انواع سرطان وجود ندارد.متیلاسیون DNA همیشه یک هدف اصلی مورد توجه بوده است زیرا متیلاسیون DNA معمولا قبل از سایر تغییرات ژنتیکی قابل تشخیص رخ می دهد.در حین بررسی ویژگیهای مشترک سرطان با استفاده از یک توالییابی راهنمای جدید برای متیلاسیون DNA، یک سری از نشانگرهای جهانی فقط سرطان (UCOMs) به عنوان کاندیدای قوی برای تشخیص زودهنگام موثر و دقیق سرطان ظاهر شدهاند.در حالی که ارزش بالینی نشانگرهای زیستی سرطان فعلی به دلیل حساسیت کم و/یا ویژگی کم کاهش می یابد، ویژگی های منحصر به فرد UCOM نتایج معنی دار بالینی را تضمین می کند.اعتبارسنجی پتانسیل بالینی UCOM ها در سرطان های ریه، دهانه رحم، آندومتر و اوروتلیال بیشتر از کاربرد UCOM در انواع سرطان ها و سناریوهای مختلف بالینی پشتیبانی می کند.در واقع، کاربردهای UCOM در حال حاضر تحت بررسی فعال با ارزیابی بیشتر در تشخیص زودهنگام سرطان، تشخیص کمکی، اثربخشی درمان و نظارت بر عود هستند.مکانیسم های مولکولی که توسط آن UCOM ها سرطان ها را تشخیص می دهند موضوعات مهم بعدی هستند که باید بررسی شوند.استفاده از UCOM در سناریوهای دنیای واقعی نیز نیازمند اجرا و اصلاح است.
کلید واژه ها
تشخیص سرطان؛غربالگری سرطان؛متیلاسیون DNA؛اپی ژنتیک سرطان؛نشانگرهای زیستی سرطان
چرا ما نیاز فوری به جدید داریم نشانگرهای زیستی؟
پس از بیش از یک قرن مبارزه با سرطان، سرطان همچنان کشنده ترین تهدید بیولوژیکی برای بشر است.سرطان با 19.3 میلیون مورد جدید و نزدیک به 10 میلیون مرگ تخمین زده شده در سال 20201، یک نگرانی بهداشت جهانی باقی مانده است. در سال 2020 حدود 4.6 میلیون مورد جدید سرطان در چین تشخیص داده شد که بر اساس GLOBOCAN1 23.7 درصد از موارد جدید سرطان در جهان را تشکیل می دهد.علاوه بر این، در سال 2020، تقریباً 3 میلیون مرگ ناشی از سرطان در چین نسبت داده شد که 30 درصد از مرگ و میرهای جهانی مرتبط با سرطان را تشکیل می داد.این آمار نشان میدهد که چین رتبه اول را در میزان بروز و مرگ و میر سرطان دارد.علاوه بر این، نرخ بقای 5 ساله سرطان 40.5٪ است که 1.5 برابر کمتر از نرخ بقای 5 ساله در ایالات متحده است.بقای نسبتاً پایین تر و نرخ مرگ و میر بالاتر در چین نسبت به کشورهایی که شاخص های توسعه انسانی بالاتری دارند، نشان می دهد که یک سیستم پیشگیری و نظارت بر سرطان کارآمد و مقرون به صرفه نیاز فوری دارد.تشخیص زودهنگام سرطان یکی از حیاتی ترین عناصر در سیستم مراقبت های بهداشتی است.تشخیص زودهنگام سرطان می تواند پیش آگهی و بقا را در مراحل اولیه تقریباً در همه انواع سرطان بهبود بخشد.استراتژی های غربالگری موفق منجر به کاهش قابل توجهی در میزان بروز و مرگ و میر سرطان های دهانه رحم، پستان، کولورکتال و پروستات شده است.
با این حال، دستیابی به تشخیص زودهنگام سرطان کار آسانی نیست.بررسی زیستشناسی و پیشآگهی سرطان اولیه، شناسایی و اعتبارسنجی نشانگرهای زیستی تشخیص زودهنگام قابل اعتماد، و توسعه فناوریهای تشخیص زودهنگام در دسترس و دقیق، همیشه بزرگترین موانع در این فرآیند بوده است.تشخیص دقیق سرطان می تواند ضایعات خوش خیم را از بدخیم تشخیص دهد که به جلوگیری از اقدامات غیر ضروری و تسهیل مدیریت بیشتر بیماری کمک می کند.استراتژیهای تشخیص زودهنگام کنونی شامل بیوپسیهای مبتنی بر آندوسکوپ، تصویربرداری پزشکی، سیتولوژی، سنجشهای ایمنی و تستهای نشانگرهای زیستی 5-7 است.بیوپسی های مبتنی بر آندوسکوپ، به دلیل مزاحم و پرهزینه بودن، بار ذاتاً سنگینی را به عنوان یک روش اصلی پزشکی با تکیه بر پرسنل حرفه ای حمل می کنند.مانند سیتولوژی، هر دو روش غربالگری به متخصصان پزشکی بستگی دارد و بر اساس قضاوت شخصی با عملکردی دور از ایده آل است.در مقابل، با توجه به نرخ مثبت کاذب بالا، ایمونواسی بسیار نادرست هستند.تصویربرداری پزشکی به عنوان یک تاکتیک غربالگری به تجهیزات گران قیمت و تکنسین های متخصص نیاز دارد.از این رو، تصویربرداری پزشکی به دلیل دسترسی کم بسیار محدود است.به همه این دلایل، نشانگرهای زیستی گزینه بهتری برای تشخیص زودهنگام سرطان هستند.
مکاتبه با: یینشان لی و ونچیانگ یو
Email: liyinshan@nxrmyy.com and wenqiangyu@fudan.edu.cn
شناسه ORCID: https://orcid.org/0009-0005-3340-6802 و
https://orcid.org/0000-0001-9920-1133
دریافت در 22 آگوست 2023;پذیرش در 12 اکتبر 2023؛
منتشر شده آنلاین در 28 نوامبر 2023.
موجود در www.cancerbiomed.org
©2023 بیولوژی و پزشکی سرطان.عوام خلاق
Attribution-NonCommercial 4.0 License International
بیومارکرها در حال حاضر به عنوان پروتئین ها، نشانگرهای جهش DNA، نشانگرهای اپی ژنتیکی، ناهنجاری های کروموزومی، نشانگرهای RNA که مستقیماً از تومورها مشتق شده اند یا قطعات توموری که به طور غیرمستقیم از مایعات بدن به دست می آیند، طبقه بندی می شوند.نشانگرهای پروتئینی پرکاربردترین نشانگرهای زیستی در غربالگری و تشخیص سرطان هستند.بیومارکرهای پروتئینی، به عنوان نشانگرهای زیستی غربالگری، به دلیل تمایل به تحت تأثیر قرار گرفتن ضایعات خوش خیم محدود می شوند، که منجر به تشخیص بیش از حد و درمان بیش از حد می شود، همانطور که برای α-fetoprotein و آنتی ژن اختصاصی پروستات (PSA)9،10 گزارش شده است.نشانگرهای RNA شامل الگوهای بیان ژنتیکی و سایر نشانگرهای RNA غیر کدکننده هستند. ترکیبی از نشانگرهای بیان ژنتیکی RNA را می توان با استفاده از نمونه ادرار تشخیص داد که حساسیت آن برای تومورهای اولیه بسیار رضایت بخش بود (60%) و تشخیص آن می تواند تحت تأثیر ماهیت تجزیه آسان RNA در محیط طبیعی قرار می گیرند.نشانگرهای ژنتیکی و اپی ژنتیکی هر دو با مشکل شیوع در تومورها و محدودیت در انواع سرطان مواجه هستند.
متیلاسیون DNA از زمانی که برای اولین بار توسط فاینبرگ در سال 198312 با سرطان مرتبط شد، کاندیدای قوی به عنوان یک نشانگر زیستی برای تشخیص زودهنگام بوده است.هیپرمتیلاسیون نابجای DNA معمولاً در جزایر CpG در پروموترهای ژن برای مقابله با سرکوبگرهای تومور انجام می شود.مطالعات همچنین نشان دادهاند که هیپرمتیلاسیون غیرطبیعی DNA در تنظیمکنندههای رشدی دخیل است.دره متیلاسیون DNA، که معمولاً با تنظیمکنندههای رشد و سرطانهای هیپرمتیله مرتبط است، ممکن است حالت بیان ژن را به حالت وابسته به متیلاسیون DNA پایدارتر تغییر دهد و اتصال به هیستون متیله H3K27me3 و پروتئینهای پلیکامب مرتبط را کاهش دهد.
در میان تعداد زیادی از نشانگرهای متیلاسیون DNA منتشر شده، چندین مورد با موفقیت در بازار عرضه شده اند.با این حال، نشانگرهای متیلاسیون DNA تجاری و پانل های تشخیصی فعلی هنوز به دلایل متعدد پتانسیل تشخیص زودهنگام سرطان را به طور کامل باز نکرده اند.این نشانگرهای زیستی در حالی که عمدتاً عملکرد قابل قبولی را با استفاده از اطلاعات پایگاه داده نشان میدهند، معمولاً به دلیل این واقعیت که نمونههای دنیای واقعی اغلب پیچیدهتر هستند و به اندازه نمونههای انتخاب شده در پایگاههای داده نماینده نیستند، عملکرد ایدهآلتری در دنیای واقعی دارند.تشخیص زودهنگام متیلاسیون چند سرطانی مبتنی بر توالی یابی نسل بعدی نشان داده شده است که به ترتیب در سرطان های مرحله I و II حساسیت 16.8% و 40.4% دارد.آزمایشهای تشخیص زودهنگام به پایداری بیشتر و نشانگرهای زیستی دقیقتر نیاز دارند.
کشف نشانگر جهانی سرطان (UCOM) با استفاده از توالی موقعیت یابی راهنما (GPS)
با وجود دههها تحقیق درباره سرطان، پیشگیری و درمان رضایتبخشی محقق نشده است.روشهای جدیدی مورد نیاز است تا محققان بتوانند سرطان را به طور کامل ارزیابی کنند.در طول 23 سال گذشته، 6 نشانه سرطان، مانند اجتناب از آپوپتوز، تهاجم بافتی و متاستاز، و غیره، با گنجاندن ویژگیهایی مانند برنامهریزی مجدد اپی ژنتیکی غیرجهشی و میکروبیومهای چندشکلی به 14 مورد افزایش یافته است.همانطور که جزئیات بیشتر مربوط به سرطان فاش می شود، دیدگاه های بیشتری به تحقیقات سرطان معرفی می شود.تحقیقات سرطان به تدریج در دو جهت (مشترکی و فردیت) وارد دوره جدیدی شده است.با توسعه انکولوژی دقیق در سال های اخیر، تمرکز تحقیقات سرطان به سمت درمان هدفمند فردی و ناهمگونی سرطان متمایل شده است.بنابراین، نشانگرهای زیستی سرطان که اخیراً شناسایی شدهاند، عمدتاً بر انواع سرطانهای خاص، مانند سرطان اجباری PAX623 و BMP3 برای سرطان کولورکتال تمرکز کردهاند.عملکرد این نشانگرهای زیستی خاص برای انواع سرطان متفاوت است، اما به دلیل محدودیت در تهیه نمونه بیولوژیکی و هزینه بالا، هنوز برای افراد مستعد امکان غربالگری برای همه سرطانها به طور همزمان وجود ندارد.اگر بتوانیم یک نشانگر زیستی منفرد و قوی را شناسایی کنیم که برای همه انواع سرطان در مرحله اولیه موثر است، ایده آل خواهد بود.
برای دستیابی به چنین هدف ایده آلی، یک نامزد نشانگر زیستی بهتر باید از لیست انواع بیومارکرهای بالقوه انتخاب شود.انحرافات متیلاسیون DNA، در میان تمام مشخصات ژنتیکی و اپی ژنتیکی، به عنوان مرتبط با سرطان شناخته شده است و برخی از اولین، اگر نه اولین، ناهنجاری های مرتبط با سرطان هستند که به صورت زمانی رخ می دهند.بررسی متیلاسیون DNA زود آغاز شد، اما به دلیل فقدان روش های تحقیقاتی مانع شده است.در میان 28 میلیون سایت بالقوه CpG متیله در ژنوم، تعداد قابل کنترلی باید شناسایی و با ژنوم هماهنگ شود تا تومورزایی بهتر درک شود.توالی یابی بی سولفیت کل ژنوم (WGBS)، که به عنوان استاندارد طلایی توالی یابی متیلاسیون DNA در نظر گرفته می شود، به دلیل ماهیت درمان با بی سولفیت که باعث شکسته شدن قطعات DNA و کاهش پیچیدگی ژنوم در طول زمان می شود، تنها می تواند 50 درصد از Cs در سلول های سرطانی را پوشش دهد. تبدیل Cs-به-Ts25.روش های دیگر، مانند تراشه های 450 هزار، تنها 1.6 درصد متیلاسیون ژنوم را پوشش می دهند.بر اساس 450 هزار داده، یک پانل تشخیص متیلاسیون DNA برای 6 نوع سرطان مرحله I 35.4 درصد حساسیت دارد.محدودیتهای انواع سرطان، عملکرد ضعیف و نویز ایجاد شده توسط روشهای تشخیص در فرآیند تحلیلی به بزرگترین موانع برای پانلهای تشخیص پان سرطان تبدیل شدهاند.
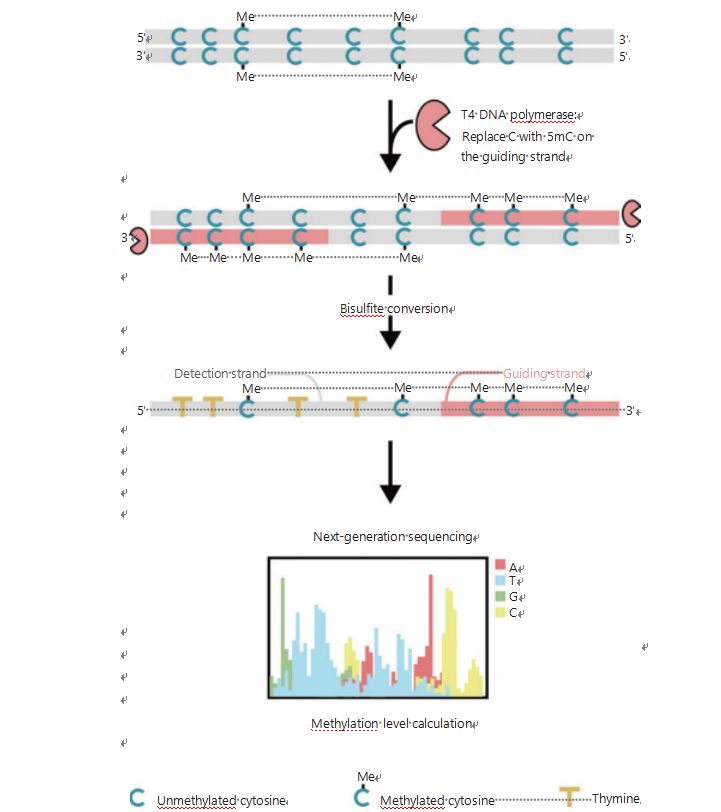
برای بررسی بهتر الگوهای اپی ژنتیکی سلولها در طول تومورزایی و متاستاز، ما یک GPS منحصربهفرد برای تشخیص متیلاسیون DNA در سطح ژنوم ایجاد کردیم که تا 96% از سایتهای CpG را در 0.4 میلیارد مطالعه پوشش میدهد.GPS یک روش توالی یابی دو طرفه با استفاده از یک انتهای 3' قطعه DNA متیل سیتوزین های غیر قابل تبدیل پس از تصفیه بی سولفیت است که همسویی محاسبه متیلاسیون DNA انتهای 5' را از طریق توالی یابی جفت انتهایی هدایت می کند (شکل 1)25.رشته هدایت کننده متیل سیتوزین، که به عنوان یک رشته الگو عمل می کند، به هم ترازی ناحیه با GC بالا کمک می کند که بیشترین داده های توالی یابی رها شده را در WGBS سنتی بازیابی می کند.ویژگی پوشش بالای GPS مقدار زیادی از اطلاعات متیلاسیون DNA را فراهم می کند که به ما امکان می دهد پروفایل های متیلاسیون سرطان را با وضوح قابل توجهی بالاتر در مناطقی که قبلاً بررسی نشده بود بررسی کنیم.
GPS ابزار قدرتمندی برای بررسی همگنی سرطان در اختیار ما قرار می دهد، که می تواند تحقیقات سرطان را تا حد زیادی ساده کند و به طور بالقوه توضیحی جهانی برای تومورزایی و متاستاز پیدا کند.هنگام تجزیه و تحلیل داده های GPS خطوط سلولی سرطانی، پدیده منحصر به فردی به طور مکرر با آن مواجه شد.تعدادی از مناطق وجود داشت که به نظر می رسید در انواع مختلف نمونه های سرطانی به طور غیر طبیعی هیپرمتیله شده بودند.این یافته غیرمنتظره متعاقباً برای خدمت به عنوان UCOM تأیید شد.بیش از 7000 نمونه از 17 نوع سرطان در پایگاه داده اطلس ژنوم سرطان (TCGA) مورد تجزیه و تحلیل قرار گرفته است که در میان آنها ما اولین UCOM، HIST1H4F، یک ژن مرتبط با هیستون را شناسایی کردیم که در همه انواع سرطان هایپرمتیله می شود.سپس مجموعهای از UCOMها در پایگاه داده TCGA، پایگاه داده ژن بیان Omnibus (GEO) و نمونههای بالینی دنیای واقعی یافت و تأیید شدند.در حال حاضر، HIST1H4F، PCDHGB7، و SIX6 به عنوان UCOM پیدا و تایید شده اند.کشف غیرمنتظره UCOM ها پاسخی قدرتمند به نیاز به تشخیص زودهنگام سرطان ارائه می دهد.UCOM ها راه حلی برای تشخیص تک نشانگر سرطان های متعدد ارائه می دهند.
ویژگی های UCOM
پس از اعتبارسنجی، نشان داده شده است که UCOM ها چهار ویژگی اصلی را نشان می دهند که UCOM ها را قادر می سازد از کارایی نشانگرهای زیستی فعلی پیشی بگیرند (شکل 2).
منحصر به فرد برای بدخیمی
UCOM ها منحصر به ضایعات سرطانی یا پیش سرطانی هستند و تحت تأثیر تغییرات فیزیولوژیکی طبیعی قرار نمی گیرند.برخی از نشانگرهای مرتبط با سرطان که به طور گسترده در تشخیص زودهنگام و/یا غربالگری به کار گرفته شده اند، منجر به تشخیص بیش از حد شده اند.افزایش سطح PSA، یک ابزار غربالگری معتبر بالینی، در شرایط خوش خیم مانند هیپرپلازی پروستات و پروستاتیت نیز شناسایی می شود.تشخيص بيش از حد و درمان بيش از حد در نتيجه منجر به كاهش كيفيت زندگي ناشي از عوارض رودهاي، ادراري و جنسي ميشود.سایر نشانگرهای زیستی مبتنی بر پروتئین و به طور گسترده مورد استفاده در محیط بالینی، مانند CA-125، در حالی که تشخیص بیش از حد و درمان بیش از حد انجام می شود، هیچ مزیت قابل توجهی به همراه نداشته است.ویژگی بالای UCOM برای بدخیمی ها از این کاستی ها جلوگیری می کند.UCOM، PCDHGB7، ضایعات داخل اپیتلیال سنگفرشی درجه بالا (HSILs) و سرطان دهانه رحم را از نمونه های طبیعی و ضایعات داخل اپیتلیالی سنگفرشی درجه پایین (LSILs) به طور موثر متمایز می کند، در حالی که بیشتر نشانگرهای زیستی دیگر فقط می توانند سرطان دهانه رحم را از نمونه های طبیعی متمایز کنند.اگرچه PCDHGB7 تفاوت های قابل توجهی را بین آندومتر طبیعی و هیپرپلازی آندومتر تشخیص نمی دهد، تفاوت های قابل توجهی بین آندومتر طبیعی و هیپرپلازی آتیپیک تشخیص داده می شود، و حتی تفاوت های بزرگ تری بین آندومتر طبیعی و سرطان آندومتر (EC) بر اساس PCDHGB731 تشخیص داده می شود.UCOM ها منحصر به ضایعات بدخیم در پایگاه داده ها و نمونه های بالینی هستند.از دیدگاه بیمار، UCOMهای منحصربهفرد آستانه درک نشانههای پیچیده نشانگرهای زیستی ناپایدار مختلف با عملکرد ضعیف و اضطراب مربوطه را در طول فرآیند ارزیابی کاهش میدهند.از دیدگاه پزشک، UCOMهای منحصربهفرد بدخیمیها را از ضایعات خوشخیم متمایز میکنند که به تریاژ بیماران کمک میکند و اقدامات پزشکی غیر ضروری و درمان بیش از حد را کاهش میدهد.بنابراین، UCOMهای منحصر به فرد، افزونگی سیستم پزشکی را کاهش می دهند، پریشانی سیستم را تسکین می دهند و منابع پزشکی بیشتری را در اختیار نیازمندان قرار می دهند.
شکل 1 شماتیک گردش کار GPS برای تشخیص متیلاسیون DNA25.خط خاکستری: توالی DNA ورودی.خط قرمز: DNA تیمار شده با T4 DNA پلیمراز، جایگزینی سیتوزین با 5'-methylcytosine در انتهای 3' ورودی.C آبی با من: سیتوزین متیله.آبی C: سیتوزین غیر متیله.T زرد: تیمین 25.
همه یا هیچ
UCOM ها فقط در سلول های سرطانی وجود دارند و تقریباً در تمام سلول های سرطانی به طور پایدار شناسایی می شوند.HIST1H4F تقریباً در تمام انواع تومورهای هیپرمتیله شده تأیید شد، اما در نمونههای طبیعی نه.به طور مشابه، PCDHGB7 و SIX6 نیز نشان داده شده است که در همه نمونههای تومور هیپرمتیله شدهاند، اما در نمونههای عادی 30-32 وجود ندارد.این ویژگی منحصر به فرد به طور قابل توجهی عملکرد UCOM ها را با توجه به محدودیت تشخیص و حساسیت بهبود می بخشد.تنها 2 درصد از سلولهای سرطانی را میتوان در نمونهها تمایز داد، که UCOMs را به یک نشانگر زیستی بسیار حساستر از بسیاری از نشانگرهای زیستی موجود تبدیل میکند. پیشنهاد پتانسیل تشخیصی ضعیف33.شیوع کم جهش های KRAS در سرطان کولورکتال، KRAS را در ترکیب با سایر نشانگرهای زیستی محدود می کند.در واقع، ترکیبی از نشانگرهای زیستی ممکن است در ابتدا امیدوارکننده به نظر برسد، اما همیشه نتیجه رضایتبخشی ایجاد نمیکند در حالی که نویز بسیار بیشتری را در تجزیه و تحلیل تشخیص نشان میدهد و معمولاً شامل روشهای آزمایشی پیچیدهتر است.در مقابل، PCDHGB7 و سایر UCOM ها در همه سرطان ها وجود دارند.UCOMها اجزای سرطانی را در انواع مختلف نمونههای سرطان با نهایت دقت شناسایی میکنند و در عین حال فرآیندهای پیچیده آنالیز حذف نویز را ریشه کن میکنند.تشخیص سرطان در یک نمونه فراوان دشوار نیست، اما تشخیص سرطان در یک نمونه کوچک بسیار چالش برانگیز است.UCOM ها قادر به تشخیص مقادیر کمی سرطان هستند.
شکل 2 ویژگی های UCOM.
تشخیص سرطان قبل از تغییرات پاتولوژیک
UCOM ها را می توان در مرحله پیش سرطانی قبل از تغییرات پاتولوژیک شناسایی کرد.به عنوان نشانگرهای زیستی اپی ژنتیک، ناهنجاریهای UCOM در مراحل اولیهتری نسبت به ناهنجاریهای فنوتیپی رخ میدهند و در طول تومورزایی، پیشرفت و متاستاز قابل تشخیص هستند34،35.حساسیت UCOM در طول زمان باعث افزایش عملکرد UCOM در تشخیص سرطان در مراحل اولیه و ضایعات پیش سرطانی می شود.تشخیص زودهنگام سرطان بر اساس بیوپسی و سیتولوژی حتی برای باتجربه ترین آسیب شناسان نیز می تواند دشوار باشد.یک بیوپسی منفرد به دست آمده از طریق کولپوسکوپی در 60.6 درصد از نمونه های HSIL+ مثبت گزارش شده است.بیوپسی های اضافی برای ضایعات متعدد برای افزایش حساسیت مورد نیاز است.در مقابل، UCOM، PCDHGB7، دارای حساسیت 82 درصدی برای نمونه های HSIL+ است که از حساسیت نمونه برداری ها و بیشتر نشانگرهای زیستی فراتر می رود.نشانگر متیلاسیون، FAM19A4، دارای حساسیت 69٪ برای CIN2+ است که مشابه سیتولوژی است، اما نمی تواند CIN1 را از نمونه های معمولی متمایز کند37.نشان داده شده است که UCOM ها نشانگر زیستی تشخیص زودهنگام بسیار حساس تری هستند.در مقایسه با پاتولوژیستهای مبتنی بر تجربه، UCOMها حساسیت تشخیص بالاتری برای سرطانهای در مراحل اولیه دارند که به نوبه خود به بهبود پیشآگهی سرطان و بقا کمک میکند.علاوه بر این، UCOM ها یک پلت فرم تشخیص ارائه می دهند که برای مناطقی که آسیب شناسان مجرب ندارند قابل دسترسی است و کارایی تشخیص را تا حد زیادی بهبود می بخشد.با روشهای نمونهبرداری و شناسایی یکنواخت، تشخیص UCOM نتایج پایدار و قابل تفسیری را به دست میدهد که با پروتکل غربالگری که به پرسنل حرفهای و منابع پزشکی کمتری نیاز دارد، مناسبتر است.
تشخیص آسان
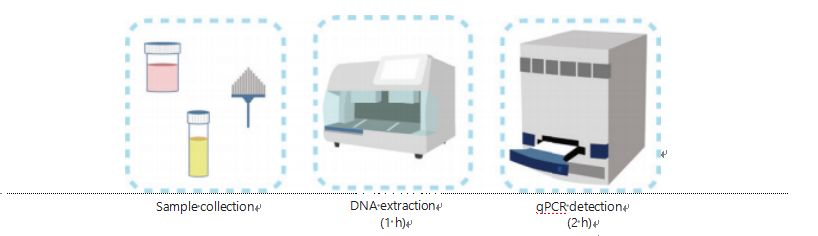
روش های فعلی برای تشخیص متیلاسیون DNA پیچیده و زمان بر هستند.اکثر روش ها نیاز به تبدیل بی سولفیت دارند که باعث کاهش کیفیت نمونه و احتمالاً نتایج ناپایدار و نادرست می شود.تکرارپذیری ضعیف ناشی از درمان بی سولفیت به طور بالقوه منجر به سردرگمی پزشکان و بیماران می شود و بیشتر با راهبردهای پیگیری و/یا درمان تداخل می کند.بنابراین، ما روش تشخیص UCOM را برای جلوگیری از درمان مشکل ساز بی سولفیت نمونه ها، تطبیق با الزامات کاربرد بالینی و افزایش دسترسی اصلاح کردیم.ما یک روش جدید را با استفاده از آنزیمهای محدودکننده حساس به متیلاسیون همراه با PCR کمی فلورسنت بلادرنگ (Me-qPCR) برای تعیین کمیت وضعیت متیلاسیون UCOMs در عرض 3 ساعت با استفاده از روشهای جابجایی آسان ایجاد کردیم (شکل 3).Me-qPCR میتواند انواع مختلفی از نمونهها، مانند جمعآوری بالینی مایعات بدن و نمونههای ادرار جمعآوریشده را در خود جای دهد.نمونههای بالینی جمعآوریشده را میتوان پردازش، ذخیره کرد و با استفاده از استخراج DNA استاندارد و خودکار، به راحتی به تشخیص ادامه داد.سپس DNA استخراجشده را میتوان مستقیماً به پلتفرم Me-qPCR برای واکنش یک گلدانی و نتایج کمیسازی خروجی اعمال کرد.پس از تجزیه و تحلیل نتایج ساده با استفاده از مدلهای تشخیصی برازش و تایید شده برای انواع سرطان خاص، تعیین نهایی نتایج تشخیص UCOM تفسیر شده و به عنوان یک مقدار نیمه کمی ارائه میشود.طبق پروتکل کیت EZ DNA Methylation-Gold، پلت فرم Me-qPCR در تشخیص UCOM عملکرد بهتری نسبت به بی سولفیت-پیروزهیابی سنتی دارد و در عین حال 3 ساعت در تبدیل بی سولفیت صرفهجویی میکند.پلت فرم نوآورانه تشخیص متیلاسیون، تشخیص UCOM را پایدارتر، دقیق تر و در دسترس تر می کند30.
شکل 3 فرآیند شناسایی UCOM ها.انواع نمونه عبارتند از BALF نمونه برداری حرفه ای، برس پاپ و/یا ادرار جمع آوری شده توسط خود.فرآیند استخراج DNA را می توان با یک استخراج کننده خودکار تطبیق داد که محصول آن مستقیماً توسط qPCR قابل شناسایی است.
کاربرد UCOM ها
سرطان ریه
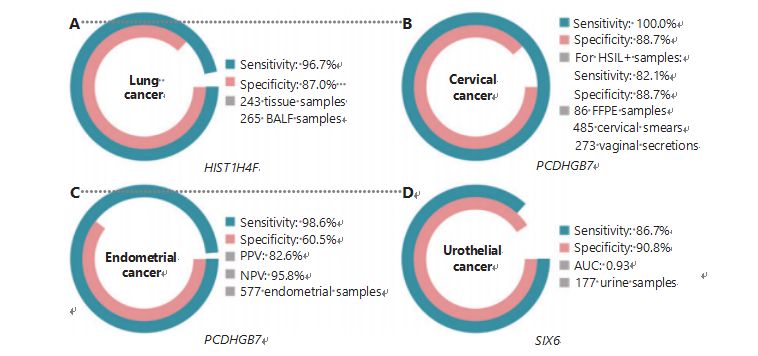
سرطان ریه دومین سرطان شایع و کشنده ترین سرطان در سراسر جهان است که 11.4 درصد موارد جدید و 18.0 درصد مرگ و میرهای جدید را به خود اختصاص داده است.در بین تمام تشخیصها، 85 درصد سرطان ریه سلول غیرکوچک (NSCLC) و 15 درصد سرطان ریه سلول کوچک (SCLC) است که سطح بدخیمی بالاتری دارد.اسکن توموگرافی کامپیوتری با دوز پایین (LDCT) روش غربالگری توصیه شده در حال حاضر برای سرطان ریه است و نشان داده شده است که تشخیص زودهنگام و کاهش مرگ و میر را بهبود می بخشد.با این حال، به دلیل ویژگی کم و دسترسی ضعیف، LDCT هنوز به عنوان یک روش غربالگری رضایت بخش عمل نکرده است، مانند سایر نشانگرهای سرطانی رایج، مانند CEA39.هزینهها و پتانسیل تشخیصهای از دست رفته و تشخیصهای اشتباه استراتژی غربالگری LDCT مانع از پیشرفت ترویج غربالگری سرطان ریه میشود.HIST1H4F، یک UCOM، دارای پتانسیل بسیار زیادی به عنوان نشانگر زیستی تشخیص زودهنگام در نمونه های مایع برونش آلوئولار (BALF) است.HIST1H4F در آدنوکارسینوم ریه و کارسینوم سلول سنگفرشی ریه، با ویژگی تشخیص 96.7% و حساسیت 87.0% (شکل 4A) و عملکرد استثنایی برای سرطان های مرحله I27، هیپرمتیله می شود.HIST1H4F دارای ویژگی 96.5٪ و حساسیت 85.4٪ برای NSCLC، و 96.5٪ و 95.7٪ برای SCLC27 است.علاوه بر این، نمونههایی از هشت نوع سرطان دیگر، از جمله سرطان پانکراس و کولورکتال، تأیید کردهاند که HIST1H4F در هر هشت نوع هیپرمتیله شده است.
سرطان دهانه رحم
سرطان دهانه رحم چهارمین سرطان شایع تشخیص داده شده و چهارمین علت اصلی مرگ و میر ناشی از سرطان در زنان در سال 2020 بوده است که 3.1 درصد موارد جدید و 3.4 درصد از مرگ و میرهای مرتبط با سرطان را در سراسر جهان به خود اختصاص داده است.برای از بین بردن سرطان دهانه رحم تا سال 2030، همانطور که توسط WHO پیشنهاد شده است، تشخیص زودهنگام سرطان دهانه رحم یک ضرورت است.اگر در مراحل اولیه تشخیص داده شود، میزان بقای 5 ساله با سرطان مهاجم دهانه رحم به 92 درصد می رسد.دستورالعملهای انجمن سرطان آمریکا (ACS) آزمایشهای سیتولوژی دهانه رحم، آزمایشهای HPV اولیه یا آزمونهای مشابه را برای غربالگری پیشنهاد میکند.سیتولوژی دهانه رحم تهاجمی است و تنها می تواند 63.5٪ موارد CIN2+ را تشخیص دهد.
در مقابل، PCDHGB7 با استفاده از پاپ اسمیر و ترشحات واژینال بسیار بهتر عمل کرده است و می تواند به طور موثر HSIL را از LSIL در مراحل بسیار اولیه متمایز کند.PCDHGB7 به تنهایی دارای حساسیت 100.0٪ و ویژگی 88.7٪ برای سرطان دهانه رحم (شکل 4B) و حساسیت 82.1٪ و ویژگی 88.7٪ برای نمونه های HSIL+30 است.PCDHGB7 همچنین دارای 90.9 درصد حساسیت و 90.4 درصد ویژگی در نمونه های ترشح واژن برای سرطان دهانه رحم است که جمع آوری آنها بسیار آسان تر است.زمانی که PCDHGB7 با تست پرخطر (hr) HPV یا تست سیتولوژی Thinprep (TCT) ترکیب شود، حساسیت 95.7٪ و ویژگی 96.2٪ افزایش یافته است، به طور قابل توجهی از تست hrHPV (20.3٪)، TCT (51.2٪) بیشتر است. و این دو با هم (57.8%) برای سرطان دهانه رحم30.همچنین نشان داده شده است که PCDHGB7 در 17 نوع سرطان از پایگاه داده TCGA هیپرمتیله شده است که نشان دهنده مناسب بودن آن در خانواده UCOM30 است.
شکل 4 UCOM ها در چهار نوع سرطان در مطالعات بالینی در مقیاس بزرگ تایید شده اند.الف. عملکرد HIST1H4F، یک UCOM، در تشخیص سرطان ریه 508 نمونه.ب. عملکرد PCDHGB7، یک UCOM، در تشخیص سرطان دهانه رحم 844 نمونه.ج. عملکرد PCDHGB7، یک UCOM، در تشخیص سرطان آندومتر از 577 نمونه برس پاپ و تائو آندومتر.D. عملکرد SIX6، یک UCOM، در تشخیص سرطان ادراری 177 نمونه.
EC
EC یکی از شایعترین سرطانهای دستگاه تناسلی زنان در سرتاسر جهان است که سالانه 4.2 میلیون مورد جدید و 1 درصد مرگومیرهای مرتبط با سرطان تخمین زده میشود.با تشخیص موفقیت آمیز در مرحله اولیه، EC قابل درمان است و نرخ بقای 5 ساله 95٪ برای سرطان مرحله I دارد.بیمارانی که علامت دار هستند، مانند خونریزی غیرطبیعی رحم، ارزیابی بالینی دوره ای دریافت می کنند و تحت روش های بیوپسی تهاجمی و دردناک قرار می گیرند، علیرغم اینکه تنها 5٪ تا 10٪ در نهایت EC43 ایجاد می کنند.اولتراسوند ترانس واژینال، به عنوان روش رایج تشخیص، به دلیل ناتوانی در افتراق تغییرات خوش خیم از بدخیم آندومتر و نرخ بالای مثبت کاذب، بسیار غیر قابل اعتماد است.
مقایسه موازی سرم CA-125، نشانگر زیستی EC که به طور گسترده پیاده سازی شده و PCDHGB7 انجام شد.سرم CA-125 دارای حساسیت 24.8٪ بود که نشان می دهد CA-125 یک نشانگر ناکافی برای EC با وجود ویژگی 92.3٪ 31 است.تشخیص PCDHGB7 با استفاده از نمونههای برس پاپ، حساسیت 80.65% و ویژگی 82.81% را برای مراحل ECatall به همراه داشت، در حالی که برس Tao دارای حساسیت 61.29% و ویژگی 95.31% 31 بود.مدل تشخیصی PCDHGB7، بر اساس Me-qPCR، حساسیت 98.61٪، ویژگی 60.5٪، و دقت کلی 85.5٪، با استفاده از نمونه های Pap و Tao brush (شکل 4C)31 به دست آورد.
سرطان اروتلیال
سرطان اروتلیال، متشکل از سرطانهای مثانه، لگن کلیه و حالب، هفتمین سرطان شایع در سال 2020 در سراسر جهان بود که باعث 2/5 درصد موارد جدید و 9/3 درصد از مرگها شد.سرطان های اروتلیال که بیش از 50 درصد آنها سرطان مثانه است، چهارمین سرطان شایع در ایالات متحده در سال 2022 بود که 11.6 درصد از موارد تازه تشخیص داده شده را تشکیل می داد.تقریباً 75 درصد از سرطان های مثانه به عنوان سرطان مثانه غیر مهاجم عضلانی و محدود به مخاط یا زیر مخاط طبقه بندی می شوند.بیوپسی سیستوسکوپی استاندارد طلایی برای تشخیص سرطان ادراری است که با هیبریداسیون درجا فلورسانس (FISH) و آزمایشات سیتولوژی اجرا می شود.FISH و سیتولوژی عملکرد تشخیصی ضعیفی دارند و سیستوسکوپی نفوذی است و خطر اساسی از دست دادن ریز ضایعات، تفسیر نادرست ضایعات و به طور بالقوه ایجاد گسترش یا عود سرطان را دارد.UCOM تایید شده قبلی، PCDHGB7، همچنین نشان داده شد که در سرطان مجرای ادراری با مساحت زیر منحنی 0.86 هیپرمتیله شده است که نشان دهنده یک قابلیت تشخیصی بالقوه است.برای تایید بیشتر UCOM های بیشتر و تطبیق بهتر انواع نمونه، SIX6، یک UCOM جدید، مورد بررسی قرار گرفت و پتانسیل تشخیصی عالی در تشخیص زودهنگام سرطان ادراری با استفاده از نمونه های ادرار بر روی پلت فرم Me-qPCR نشان داد.تشخیص SIX6 با استفاده از نمونههای ادرار حساسیت رقابتی 86.7٪ و ویژگی 90.8٪ را نشان داد (شکل 4D)، در حالی که غیر تهاجمی و به دست آوردن آن آسان است.پتانسیل SIX6 در پایش متاستاز و ارزیابی اثربخشی درمان در حال حاضر تحت بررسی است.
آینده و چالش ها
UCOM ها عملکرد قوی در پتانسیل تشخیصی سرطان های متعدد دارند، اما کارهای زیادی برای انجام باقی مانده است.ما لیست UCOM ها را گسترش داده ایم و به طور فعال UCOM ها را در انواع بیشتری از سرطان، از جمله مواردی که به طور سنتی تشخیص آنها دشوار است، تأیید کرده ایم.نتایج اعتبارسنجی از پایگاههای داده TCGA، کاربرد UCOMs را در انواع بیشتری از سرطان و موقعیتهای بیشتری تأیید کرده است.در یک بررسی اولیه، نشان داده شده است که UCOM ها پتانسیل تشخیصی قوی برای کلانژیوکارسینوم و آدنوکارسینوم پانکراس دارند، که تشخیص آنها در مرحله اولیه با روش های غربالگری فعلی تقریباً غیرممکن است.توانایی تشخیص سرطان های نادر با UCOM ها می تواند با DNA تومور در گردش (ctDNA) توسط یک پلت فرم بیوپسی مایع بهبودیافته استفاده شود.یک مطالعه شامل پانل تشخیص پان سرطان مبتنی بر DNA پلاسما، حساسیت 57.9٪ 49 را به همراه داشت.با وجود ویژگی بالا، عملکرد کلی نشان می دهد که هنوز جای بهبود وجود دارد.
ویژگی های منحصر به فرد UCOM ها همچنین از بررسی پتانسیل UCOM در ارزیابی اثربخشی درمان و نظارت بر عود حمایت می کند.با توجه به معیارهای ارزیابی پاسخ در تومورهای جامد (RECIST)، تصویربرداری پزشکی روش توصیه شده برای نظارت بر عود و ارزیابی اثربخشی درمان است، در حالی که نشانگرهای تومور به تنهایی برای ارزیابی استفاده میشوند.با این حال، در واقعیت، رویکردهای تصویربرداری تا حد زیادی تحت تأثیر فرکانس و زمانبندی قرار میگیرند و بنابراین بیماران را در معرض خطر و هزینههای بالاتری قرار میدهند51،52.SIX6 به عنوان پیشبینیکننده متاستاز سرطان پستان تأیید شده است.نظارت بر ctDNA مبتنی بر بیوپسی مایع، نظارت در زمان واقعی را بر حداقل بیماری باقیمانده ماهها قبل از تشخیص رادیولوژیک امکانپذیر میسازد و به طور ایدهآل پیشرفت سرطان مرتبط با عود را به تاخیر میاندازد و از آن جلوگیری میکند.نتایج اولیه نشان می دهد که UCOM ها سطح هیپرمتیلاسیون سرطانی را در زمان واقعی بلافاصله پس از جراحی و درمان منعکس می کنند.حساسیت بالای نشاندادهشده توسط UCOM و کاربرد در انواع نمونههای غیر نفوذی متعدد، به UCOM اجازه میدهد تا به عنوان یک نشانگر زیستی نظارت بر عود دقیق عمل کند و در عین حال انطباق بالای بیمار را حفظ کند.
در عین حال، دسترسی عمومی به آزمون یکی دیگر از مسائل مهم است که نیاز به تلاش بیشتری دارد.در حالی که همکاریهای شناسایی UCOM در بیمارستانهای بیشتری به امید بهرهمندی از بیماران بیشتر اتخاذ شده است، تشخیصها و غربالگریهای حرفهای به طور فعال در روستاهای چین انجام شده است.UCOM ها برای واجد شرایط بودن به عنوان یک ابزار غربالگری عملی، به ویژه برای مناطق توسعه نیافته، به دسترسی بهتری نیاز دارند.
در حالی که نتایج برنامه UCOM در تشخیص زودهنگام امیدوارکننده است، ناشناخته های زیادی در مورد UCOM وجود دارد.با اکتشاف فعال، تحقیقات بیشتری در مورد اینکه چرا UCOM ها به طور جهانی در سرطان ها وجود دارند، تضمین می شود.مکانیسم های تنظیم اپی ژنتیکی زیربنایی UCOM ها ارزش بررسی بیشتر را دارند که می تواند جهت جدیدی را برای درمان سرطان توجیه کند.با بازگشت به فعل و انفعال بین همگنی و ناهمگنی تومور، ما به این موضوع علاقه مندیم که چرا UCOM ها می توانند استثنایی برای اکثر بیومارکرهای سرطانی باشند که به شدت با انواع سرطان های خاص مرتبط هستند.نقش ناهنجاری های متیلاسیون DNA شناسایی شده توسط UCOM در تومورزایی، پیشرفت تومور و متاستاز در روند از دست دادن و بازیابی هویت سلولی مشخص نشده است و نیاز به بازرسی کامل دارد.یکی دیگر از علایق اصلی در حوزه ادغام صفت همگنی UCOMها با نشانگرهای بافت منحصر به فرد به امید نزدیک شدن به تشخیص دقیق آثار سرطان و شناسایی منشاء بافت تومور به روشی معکوس نهفته است.UCOM ها می توانند ابزاری ایده آل برای پیشگیری از سرطان، تشخیص سرطان و به طور بالقوه دفاع و از بین بردن سرطان باشند.
اعطای حمایت
این کار توسط برنامه ملی تحقیق و توسعه کلیدی چین (Grant No. 2022BEG01003)، بنیاد ملی علوم طبیعی چین (Grant No. و یک کمک هزینه از موسسه علم و فناوری هزه (گرنت شماره 2021KJPT07).
بیانیه تعارض منافع
وی لی مدیر تحقیق و توسعه برای شرکت بیوتکنولوژی شانگهای Epiprobe، آموزشی ویبولیتین است.W. Yu و Epiprobe اختراعات معلق مربوط به این کار را تأیید کرده اند.همه نویسندگان دیگر هیچ منافع رقیبی را اعلام نمی کنند.
مشارکت های نویسنده
ایده و طراحی پروژه: چنگچن کیان و ونچیانگ یو.
مقاله نوشت: چنگچن کیان.
تصاویر را ساخت: چنگچن کیان.
نسخه خطی را بررسی و ویرایش کرد: Xiaolong Zou، Wei Li، Yinshan Li و Wenqiang Yu.
منابع
1. Sung H، Ferlay J، Siegel RL، LaversanneM، Soerjomataram I، Jemal A، و همکاران.آمار جهانی سرطان 2020: برآوردهای GLOBOCAN از
بروز و مرگ و میر در سراسر جهان برای 36 سرطان در 185 کشور.CA سرطان جی کلین.2021;71: 209-49.
2. Xia C، Dong X، Li H، Cao M، Sun D، He S، و همکاران.آمار سرطان در چین و ایالات متحده، 2022: پروفایل ها، روندها و عوامل تعیین کنندهChin MedJ (انگلیسی).2022;135: 584-90.
3. Siegel RL، Miller KD، WagleNS، JemalA.آمار سرطان، 2023. CA Cancer J Clin.2023;73: 17-48.
4. Crosby D، BhatiaS، Brindle KM، Coussens LM، Dive C، Emberton M، و همکاران.تشخیص زودهنگام سرطان.علوم پایه.2022;375: eaay9040.
5. Ladabaum U، Dominitz JA، KahiC، Schoen RE.استراتژی هایی برای
غربالگری سرطان کولورکتالگوارش.2020;158: 418-32.
6. Tanoue LT، Tanner NT، Gould MK، Silvestri GA.غربالگری سرطان ریهAm J Respir Crit Care Med.2015;191: 19-33.
7. Bouvard V، WentzensenN، Mackie A، Berkhof J، BrothertonJ، Giorgi-Rossi P، و همکاران.دیدگاه IARC در مورد غربالگری سرطان دهانه رحمN EnglJ Med.2021;385: 1908-18.
8. Xue P، Ng MTA، QiaoY.چالش های کولپوسکوپی برای غربالگری سرطان دهانه رحم در LMIC ها و راه حل های هوش مصنوعیBMC Med.2020;18: 169.
9. جانسون پی، ژو کیو، دائو دی، لو وای ام دی.بیومارکرهای در گردش در تشخیص و مدیریت کارسینوم کبدیNat Rev Gastroenterol Hepatol.2022;19: 670-81.
10. Van PoppelH، Albreht T، Basu P، HogenhoutR، CollenS، Roobol M. تشخیص زودهنگام سرطان پروستات مبتنی بر PSA سرم در اروپا و در سطح جهان: گذشته، حال و آینده.Nat Rev Urol.2022;19:
562-72.
11. HolyoakeA، O'Sullivan P، Pollock R، Best T، Watanabe J، KajitaY،
و همکارانتوسعه آزمایش ادرار مولتیپلکس RNA برای تشخیص و طبقه بندی کارسینوم سلول انتقالی مثانه.Clin Cancer Res.2008;14: 742-9.
12. Feinberg AP, Vogelstein B. Hypomethylation ژن های برخی سرطان های انسانی را از همتایان طبیعی آنها متمایز می کند.طبیعت.1983;301: 89-92.
13. Ng JM، Yu J. پروموتر هیپرمتیلاسیون ژن های سرکوبگر تومور به عنوان نشانگرهای زیستی بالقوه در سرطان کولورکتال.IntJ Mol Sci.2015;16: 2472-96.
14. Esteller M. اپی ژنومیک سرطان: متیلوم های DNA و نقشه های اصلاح هیستون.Nat Rev Genet.2007;8: 286-98.
15. Nishiyama A, Nakanishi M. پیمایش چشم انداز متیلاسیون DNA سرطان.روند ژنت.2021;37: 1012-27.
16. Xie W، Schultz MD، ListerR، Hou Z، Rajagopal N، Ray P، و همکاران.تجزیه و تحلیل اپی ژنومیک تمایز چند خطی سلول های بنیادی جنینی انسانسلول.2013;153: 1134-48.
17. Li Y، Zheng H، Wang Q، Zhou C، WeiL، Liu X، و همکاران.تجزیه و تحلیل های گسترده ژنوم نقش Polycomb را در ترویج هیپومتیلاسیون دره های متیلاسیون DNA نشان می دهد.ژنوم بیول.2018;19:18.
18. Koch A، JoostenSC، Feng Z، de Ruijter TC، DrahtMX، MelotteV،
و همکارانتجزیه و تحلیل متیلاسیون DNA در سرطان: مکان مورد بازدید مجدد قرار گرفت.Nat Rev Clin Oncol.2018;15: 459-66.
19. KleinEA، Richards D، Cohn A، TummalaM، Lapham R، Cosgrove D، و همکاران.اعتبار سنجی بالینی یک آزمایش تشخیص زودهنگام چند سرطانی مبتنی بر متیلاسیون هدفمند با استفاده از یک مجموعه اعتبارسنجی مستقل.ان اونکول.2021;32: 1167-77.
20. Hanahan D، Weinberg RA.علائم سرطان.سلول.2000;100: 57-70.
21. Hanahan D. نشانه های سرطان: ابعاد جدید.کشف سرطان.2022;12: 31-46.
22. شوارتزبرگ ال، کیم ES، لیو دی، شراگ دی. سرطان شناسی دقیق: چه کسی، چگونه، چه، چه زمانی، و چه زمانی نه؟کتاب آموزشی Am Soc Clin Oncol.2017: 160-9.
23. لیو اچ، منگ ایکس، وانگ جی. متیلاسیون کمی بیدرنگ
تشخیص ژن PAX1 در غربالگری سرطان دهانه رحمسرطان ژنیکول IntJ.2020;30: 1488-92.
24. Imperiale TF، RansohoffDF، Itzkowitz SH، Levin TR، Lavin P، Lidgard GP، و همکاران.آزمایش DNA چند هدف برای غربالگری سرطان کولورکتال.N EnglJ Med.2014;370: 1287-97.
25. Li J، Li Y، Li W، Luo H، Xi Y، Dong S، و همکاران.راهنمای موقعیت یابی
توالییابی الگوهای متیلاسیون DNA ناهنجار را شناسایی میکند که هویت سلولی و شبکههای نظارتی تومور-ایمنی را تغییر میدهد.ژنوم
Res.2019;29: 270-80.
26. Gao Q، LinYP، Li BS، Wang GQ، Dong LQ، Shen BY، و همکاران.تشخیص غیرمستقیم چند سرطان با توالی متیلاسیون DNA بدون سلول در گردش (THUNDER): توسعه و مطالعات تأیید مستقل.ان اونکول.2023;34: 486-95.
27. دونگ اس، لی دبلیو، وانگ ال، هو جی، سونگ ای، ژانگ بی، و همکاران.ژن های مرتبط با هیستون در سرطان ریه هیپرمتیله و هیپرمتیله می شوند
HIST1H4F می تواند به عنوان نشانگر زیستی پان سرطان عمل کند.سرطان Res.2019;79: 6101-12.
28. HeijnsdijkEA، Wever EM، AuvinenA، Hugosson J، Ciatto S، Nelen V، و همکاران.اثرات کیفیت زندگی غربالگری آنتی ژن اختصاصی پروستات.N EnglJ Med.2012;367: 595-605.
29. LuzakA، Schnell-Inderst P، Bühn S، Mayer-Zitarosa A، Siebert U. اثربخشی بالینی تستهای نشانگر بیومارکر غربالگری سرطان ارائه شده به عنوان خدمات سلامتی خود پرداخت: یک بررسی سیستماتیک.Eur J بهداشت عمومی.2016;26: 498-505.
30. دونگ اس، لو کیو، زو پی، چن ال، دوان ایکس، مائو زی، و همکاران.
PCDHGB7 Hypermethylated به عنوان یک نشانگر جهانی فقط سرطان و کاربرد آن در غربالگری اولیه سرطان دهانه رحم.Clin Transl Med.2021;11: e457.
31. Yuan J، Mao Z، Lu Q، Xu P، Wang C، Xu X، و همکاران.PCDHGB7 Hypermethylated به عنوان نشانگر زیستی برای تشخیص زودهنگام سرطان آندومتر در نمونه های برس آندومتر و خراش دادن دهانه رحم.جلو مول بیوسی.2022;8: 774215.
32. دونگ اس، یانگ زی، زو پی، ژنگ دبلیو، ژانگ بی، فو اف، و همکاران.متقابلا
اصلاح اپی ژنتیک انحصاری در SIX6 با هایپرمتیلاسیون برای ردیابی ظهور مرحله پیش سرطانی و متاستاز.هدف انتقال سیگنال در آنجا.2022;7: 208.
33. Huang L, Guo Z, Wang F, Fu L. KRAS جهش: از غیرقابل درمان به دارو در سرطان.هدف انتقال سیگنال در آنجا.2021;6: 386.
34. Belinsky SA، Nikula KJ، PalmisanoWA، MichelsR، SaccomannoG، GabrielsonE، و همکاران.متیلاسیون نابجای p16 (INK4a) یک رویداد پیش از موعد در سرطان ریه و یک نشانگر زیستی بالقوه برای تشخیص زودهنگام است.Proc Natl Acad Sci U SA.1998;95: 11891-6.
35. رابرتسون کی دی.متیلاسیون DNA و بیماری های انسانیNat Rev Genet.2005;6: 597-610.
36. WentzensenN، Walker JL، Gold MA، Smith KM، ZunaRE،
ماتیوس سی و همکارانبیوپسی های متعدد و تشخیص پیش سازهای سرطان دهانه رحم در کولپوسکوپی.جی کلین اونکول.2015;33: 83-9.
37. De Strooper LM، Meijer CJ، Berkhof J، Hesselink AT، Snijders
PJ، Steenbergen RD، و همکاران.تجزیه و تحلیل متیلاسیون FAM19A4
ژن موجود در خراش های دهانه رحم در تشخیص دهانه رحم بسیار کارآمد است
کارسینوم ها و ضایعات پیشرفته CIN2/3.سرطان قبلی (فیلا).2014;7: 1251-7.
38. تای AA، Solomon BJ، Sequist LV، Gainor JF، Heist RS.سرطان ریه.لانست.2021;398: 535-54.
39. Grunnet M، Sorensen JB.آنتی ژن کارسینومبریونیک (CEA) به عنوان نشانگر تومور در سرطان ریه.سرطان ریه.2012;76: 138-43.
40. Wood DE، KazerooniEA، Baum SL، EapenGA، EttingerDS، Hou L، و همکاران.غربالگری سرطان ریه، نسخه 3.2018، دستورالعمل های عمل بالینی NCCN در انکولوژی.J Natl Compr Canc Netw.2018;16: 412-41.
41. انجمن سرطان آمریکا.آمار و ارقام سرطانآتلانتا، GA، ایالات متحده آمریکا: انجمن سرطان آمریکا.2023 [به روز رسانی در 1 مارس 2023;به نقل از 22 اوت 2023].
42. FonthamETH، Wolf AMD، Church TR، EtzioniR، Flowers CR،
هرزیگ A و همکارانغربالگری سرطان دهانه رحم برای افراد در معرض خطر متوسط: به روز رسانی دستورالعمل 2020 از انجمن سرطان آمریکا.CA سرطان جی کلین.2020;70: 321-46.
43. Clarke MA، Long BJ، Del Mar MorilloA، Arbyn M، Bakkum-Gamez JN، Wentzensen N. ارتباط خطر سرطان آندومتر با خونریزی پس از یائسگی در زنان: بررسی سیستماتیک و متاآنالیز.JAMA Intern Med.2018;178: 1210-22.
44. جیکوبز I، جنتری-ماهاراج آ، برنل ام، مانچاندا آر، سینگ ان،
شارما A و همکارانحساسیت غربالگری سونوگرافی ترانس واژینال
برای سرطان آندومتر در زنان یائسه: مطالعه مورد-شاهدی در گروه UKCTOCSLancet Oncol.2011;12: 38-48.
45. BabjukM, Burger M, CompératEM, Gontero P, MostavidAH,
PalouJ، و همکاران.راهنمای انجمن اروپایی اورولوژی در مورد سرطان مثانه غیر تهاجمی عضلانی (TaT1 و کارسینوم درجا) -
به روز رسانی 2019.یورو اورول.2019;76: 639-57.
46. آراگون-چینگ جی بی.چالشها و پیشرفتها در تشخیص، زیستشناسی و درمان سرطانهای دستگاه ادراری فوقانی و مثانه.اورول اونکول.2017;35: 462-4.
47. Rizvi S, KhanSA, Hallemeier CL, Kelley RK, Gores GJ.
کلانژیوکارسینوم - مفاهیم در حال تکامل و استراتژی های درمانیNat Rev Clin Oncol.2018;15: 95-111.
48. Ye Q، Ling S، Zheng S، Xu X. بیوپسی مایع در سلول های کبدی
کارسینوم: سلول های تومور در گردش و DNA تومور در گردش.مول سرطان.2019;18: 114.
49. Zhang Y، Yao Y، Xu Y، Li L، Gong Y، Zhang K، و همکاران.پان سرطان
تشخیص DNA تومور در گردش در بیش از 10000 بیمار چینی.Nat Commun.2021;12:11.
50. Eisenhauer EA، Therasse P، BogaertsJ، Schwartz LH، Sargent D، Ford R، و همکاران.معیارهای ارزیابی پاسخ جدید در تومورهای جامد: دستورالعمل اصلاح شده RECIST (نسخه 1.1).Eur J سرطان.2009;45: 228-47.
51. LitièreS, Collette S, de Vries EG, Seymour L, BogaertsJ.RECIST - یادگیری از گذشته برای ساختن آینده.Nat Rev Clin Oncol.
2017;14: 187-92.
52. Seymour L، BogaertsJ، Perrone A، FordR، Schwartz LH، Mandrekar S، و همکاران.iRECIST: دستورالعمل هایی برای معیارهای پاسخ برای استفاده در کارآزمایی ها
آزمایش ایمنی درمانیLancet Oncol.2017;18: e143-52.
53. PantelK، Alix-Panabières C. بیوپسی مایع و حداقل بیماری باقیمانده - آخرین پیشرفت ها و مفاهیم برای درمان.Nat Rev Clin Oncol.2019;16: 409-24.
از این مقاله به عنوان: Qian C، Zou X، Li W، Li Y، Yu W. استناد کنید. پایگاه ضد سرطان: نشانگرهای فقط سرطان جهانی.Cancer Biol Med.2023;20: 806-815.
doi: 10.20892/j.issn.2095-3941.2023.0313
زمان ارسال: مه-07-2024